
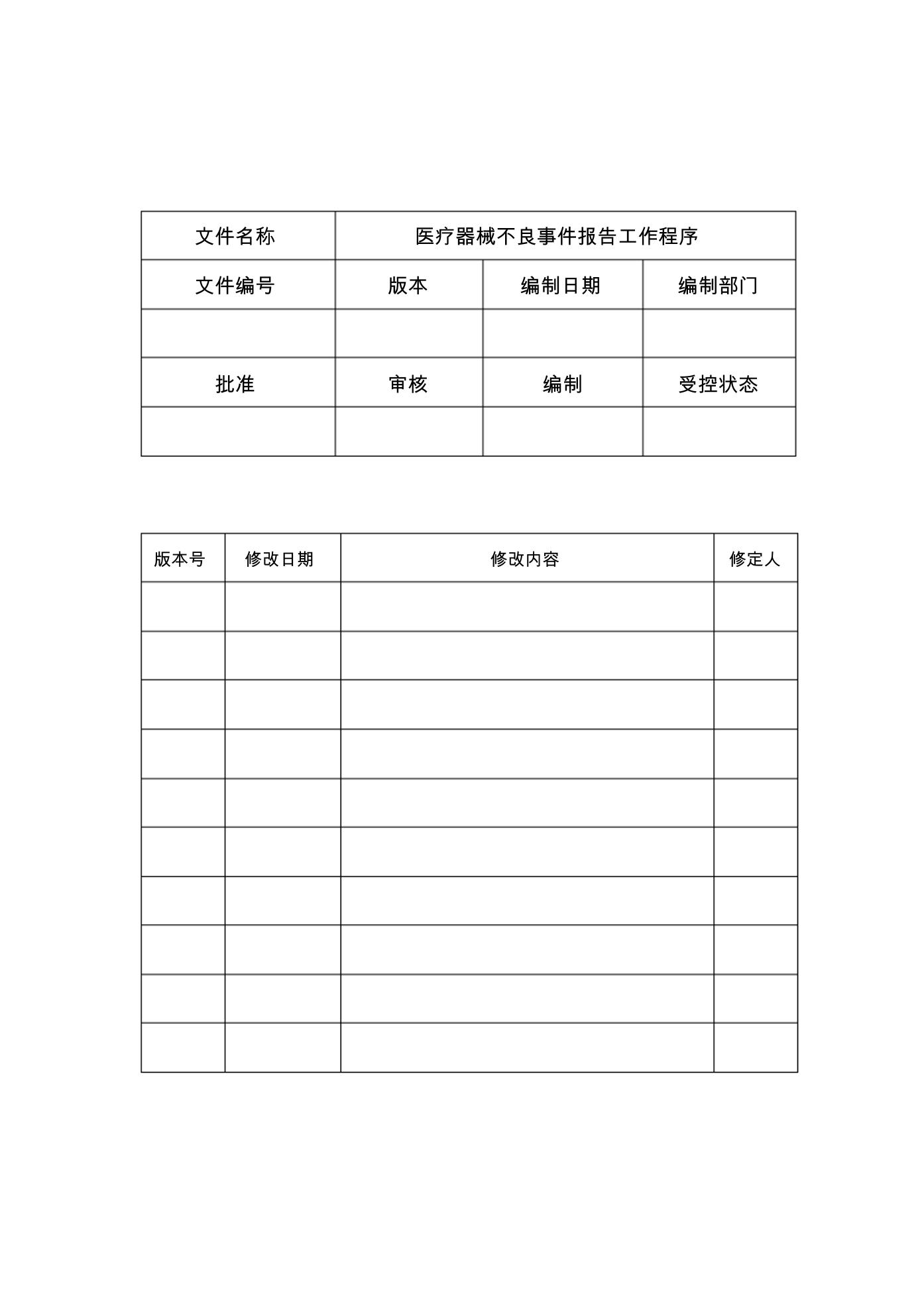
医疗器械不良事件报告工作程序
77 4.3
36 2021-01-30
pdf | 21KB | 4页
正文 简介
对不起,您暂无在线预览权限,如需浏览请
立即登录*温馨提示:该数据为用户自主上传分享,如有侵权请举报或联系客服:400-823-1298处理。
热门商品
- 2023-04-21 BUHb313534361*** 24KB 4.5
- 2023-04-21 BUHb313534361*** 42KB 4.5
- 2023-04-14 BUHb313534361*** 44KB 4.5
- 2023-04-12 chenzhipan20010*** 90KB 4.5
- 2023-04-12 chenzhipan20010*** 52KB 5
- 2023-03-06 18826288*** 576KB 5
- 2023-02-14 18826288*** 1.5MB 5
- 2022-09-16 Hc4Bq15738896*** 15KB 5
- 2022-09-07 jiang2*** 39KB 4.5
- 2022-09-07 jiang2*** 10.3MB 4.5
您可能感兴趣
原价:
100 积分
立即购买

